„Ich kann das Wasser nicht mehr halten!“ schreit „Etwas“. Das ist ein Satz, den ich von es noch nicht gehört habe.
Mit einer Mischung aus Neugier, Unruhe und Besorgnis schlurfe ich zur Küche und spähe vorsichtig hinein. Der Wasserhahn in der Spüle tropft ein bisschen, aber nicht viel. Ich möchte den Wasserhahn komplett schließen und trete in eine Pfütze. Jetzt bemerke ich, dass das Türchen unter der Spüle leicht geöffnet ist. Durch den Spalt dringen schaurige Geräusche und Flüche an meine zarten Ohren. Ich öffne die Türe komplett. Mürrisch greife ich an „Etwas“ vorbei und schließe den für Menschenhände gemachten Absperrhahn.
Disclaimer: Falls das hier von Chemikern gelesen wird, hört am besten hier auf zu lesen. Das wird euch schmerzen ersparen. Ich werde hier stark vereinfachen und auch noch das falsche Atommodell verwenden (Bohr, nicht Orbital).
Trotzdem hoffe ich, dass die Geschichte Spaß macht.
Erleichtert blickt mir „Etwas“ mit dem großen Auge entgegen. „Ups“ meint es. „Was zur Geierleier hast du denn da drinnen gemacht?“ frage ich, während ich den Tentakeln einen Mob in die Hand(?) drücke.
„Ja, ähm, ähhh, hast du gewusst, dass Wasser die einzige flüssige Verbindung aus nur zwei Gasen besteht ist?“ versucht es abzulenken.
„Ja“ „Echt?“ „Ja“ „Ok“
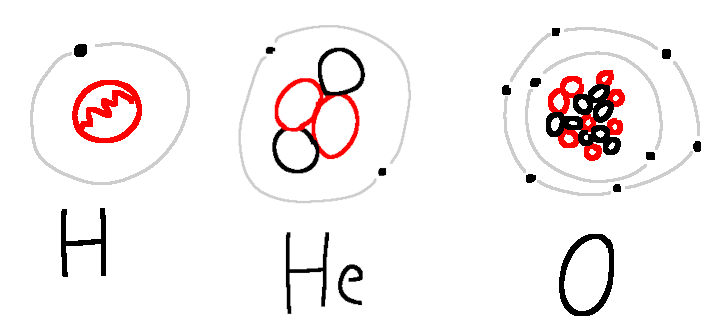
Daraufhin hole ich zum Klugscheiß-Gegenschlag aus. Wasser besteht aus zwei Wasserstoff- und einem Sauerstoff-Atom. Soweit bekannt. Die Natur ist faul und möchte möglichst ausgeglichene Verhältnisse und Gleichgewichtszustände haben. Bei Atomen bedeutet das: Am liebsten Edelgaskonfiguration. Das bedeutet, es sind alle inneren Elektronenschalen vollständig mit Elektronen gefüllt und die äußerste Schale ist mit acht Elektronen besetzt. Helium ist eine Ausnahme. Hier reichen zwei Elektronen, da es nur zwei Protonen im Kern hat. In Edelgaskonfiguration werden auf der äußeren Schale keine Elektronen aufgenommen oder abgegeben.
Mit Wasserstoff und Sauerstoff hat sich ein Atom-Pärchen gefunden bei dem ein starkes „Elektronen-Sharing“ stattfindet.
Gleichpolige Ladungen stoßen sich ab. Wie wenn man versucht, Kühlschrankmagnete mit den gleichen Polen gegeneinander zu drücken.
Trotzdem möchte Wasserstoff gerne zwei Elektronen auf seiner äußeren (und einzigen) Schale haben. Beide Teilen sich jeweils die halbe negative Ladung der zu ihnen gehörenden Elektronen. Darum liegt der Element Wasserstoff in der Natur nur in molekularer Form vor. Also als Wasserstoff-Paar (2H oder H2). So können sich beide Atome zwei Elektronen auf ihrer Schale leisten ohne nach außen hin ihre elektrische Neutralität zu verlieren.
Vereinfacht ist ein chemisches Element ein Atom aus dem sich ein Stoff zusammensetzt. Zum Beispiel Wasserstoff, Helium, Lithium, Kohlenstoff, Sauerstoff, Eisen usw. Aus den Elementen können Verbindungen Hergestellt werden. Wasser (H2O) Methan (CH4) und viele Mehr.
Sauerstoff hingegen ist nicht so friedlich. Auf seiner äußersten Elektronenschale hat es „nur“ sechs Elektronen. Aber es hätte dort gerne acht Stück um seine Edelgaskonfiguration zu erreichen. Da kommen die zwei Wasserstoff-Elektronen gerade recht. Aber das Wasserstoff-Molekül hat in seinen beiden Atomen schon seine Edelgaskonfiguration und möchte diese auch nicht wieder aufgeben. Also werden die zwei Elektronen auf der äußersten Sauerstoffschale eingegliedert, bleiben aber auch zwischen den Wasserstoffatomen geteilt. Die Wasserstoffatome gewinnen durch die zusätzlichen Elektronen des Sauerstoffs ein bisschen Freiraum und rücken ein Stück auseinander. Es entsteht ein 104° Winkel.
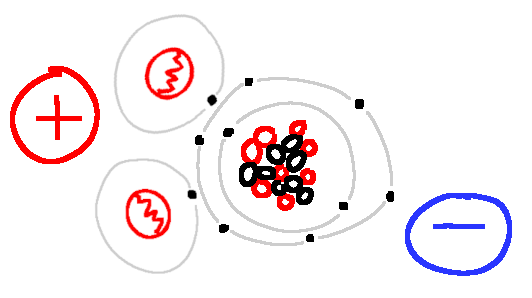
Auf der einen Seite des entstandenen Wassermoleküls haben wir jetzt mehr Elektronen als auf der anderen Seite. Dadurch entsteht eine negativ (-) und eine positiv (+) geladene Seite. Positive und negative Ladungen ziehen sich wie zwei Kühlschrankmagnete an. So kann sich Wassermolekül an Wassermolekül hängen.
Bei nur einer Handvoll zusammenhängender Moleküle haben wir gasförmiges Wasser, also Wasserdampf. Mehr zusammenhängende Moleküle bilden flüssiges Wasser. Wenn sich diese vielen Wassermoleküle dann auch noch regelmäßig anordnen, bekommen wir einen Wasserkristall aka Eis.
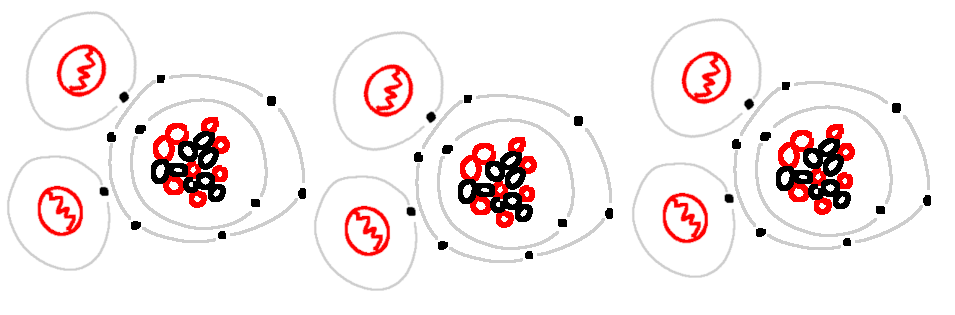
Die Menge der zusammenhängenden Moleküle hat mit deren Bewegungsenergie (Temperatur) zu tun. Vielleicht schreibe ich eventuell dazu irgendwann möglicherweise mal einen Beitrag zu diesem Thema.
Schnell mache ich einen Schritt zur Seite und versperre „Etwas“ den Weg. Es wollte meinen Monolog dazu nutzen um sich heimlich in den Kühlschrank abzusetzen.
„Du könntest das Wasser ja auf 4° Celsius abkühlen, dann ist das Volumen am geringsten und du musst weniger aufwischen“ schlage ich vor.
„Warum ist das so?“ fragt „Etwas“ und rückt dem Kühlschrank wieder ein Stückchen näher.
„Das ist witzigerweise noch nicht so ganz klar. Zum Teil hat das wieder mit der Bewegungsenergie und der asymmetrischen Ladungsverteilung in den Wassermolekülen zu tun. Bei vier Grad erreicht die elektrische Anziehung zwischen den Teilchen und deren Bewegungsdrang wieder ein Gleichgewicht. Dadurch können die Wassermoleküle maximal nahe aneinanderrücken…“ Hinter mir höre ich die Kühlschranktüre zufallen. Mist, es hat mich wieder hereingelegt.
Seufzend nehme ich den Mob und beginne die Pfütze aufzuwischen.